Cum funcționează și funcționează bateriile
 În cel mai larg sens al cuvântului în tehnologie, termenul „baterie” se referă la un dispozitiv care permite în anumite condiții de funcționare să acumuleze un anumit tip de energie, iar în altele să o folosească pentru nevoile umane.
În cel mai larg sens al cuvântului în tehnologie, termenul „baterie” se referă la un dispozitiv care permite în anumite condiții de funcționare să acumuleze un anumit tip de energie, iar în altele să o folosească pentru nevoile umane.
Ele sunt utilizate acolo unde este necesar să colectați energie pentru un anumit timp și apoi să o folosiți pentru a efectua procese mari care necesită forță de muncă. De exemplu, acumulatorii hidraulici utilizați în ecluze permit navelor să se ridice la un nou nivel pe albia râului.
Bateriile electrice funcționează cu electricitate pe același principiu: în primul rând, acumulează (acumulează) electricitate de la o sursă externă de încărcare și apoi o dau consumatorilor conectați pentru a lucra. Prin natura lor, ele aparțin surselor de curent chimic capabile să efectueze cicluri periodice de descărcare și încărcare în mod repetat.
În timpul funcționării, reacțiile chimice au loc în mod constant între componentele plăcilor cu electrozi cu substanța lor de umplere - electrolitul.
O diagramă schematică a unui dispozitiv cu baterie poate fi reprezentată printr-un desen simplificat atunci când două plăci din metale diferite cu fire sunt introduse în corpul vasului pentru a asigura contacte electrice. Între plăci se toarnă un electrolit.
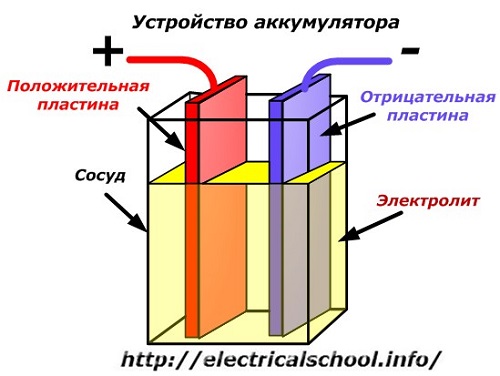
Funcționarea bateriei când este descărcată
Când o sarcină, cum ar fi un bec, este conectată la electrozi, se creează un circuit electric închis prin care curge curentul de descărcare. Se formează prin mișcarea electronilor în piesele metalice și a anionilor cu cationi în electrolit.
Acest proces este prezentat în mod convențional pe o diagramă cu un design de electrod de nichel-cadmiu.
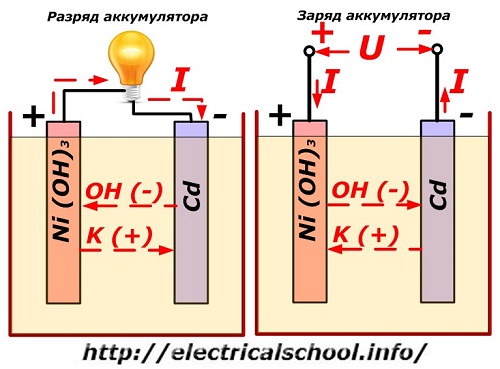
Aici, oxizii de nichel cu aditivi de grafit, care cresc conductivitatea electrică, sunt utilizați ca material al electrodului pozitiv. Metalul electrodului negativ este cadmiul spongios.
În timpul descărcării, particulele de oxigen activ din oxizii de nichel sunt eliberate în electrolit și direcționate către plăcile negative, unde cadmiul este oxidat.
Performanța bateriei la încărcare
Când sarcina este oprită, la bornele plăcii se aplică o tensiune constantă (în anumite situații, pulsatorie) de o valoare mai mare decât cea a unei baterii încărcate de aceeași polaritate, când bornele plus și minus ale sursei și ale consumatorului coincid. .
Încărcătorul are întotdeauna mai multă putere, ceea ce „suprimă” energia reziduală din baterie și creează un curent electric în sensul opus de descărcare. Ca urmare, procesele chimice interne dintre electrozi și electrolit se modifică. De exemplu, pe o cutie de plăci de nichel-cadmiu, electrodul pozitiv este îmbogățit cu oxigen, iar negativul - la o stare de cadmiu pur.
Când bateria este descărcată și încărcată, compoziția chimică a materialului plăcilor (electrozilor) se modifică, dar electrolitul nu se schimbă.
Metode de conectare a bateriei
Conexiune în paralel
Cantitatea de curent de descărcare pe care o poate suporta o persoană depinde de mulți factori, dar în primul rând de design, materialele utilizate și dimensiunile acestora. Cu cât suprafața plăcilor de la electrozi este mai mare, cu atât este mai mare curentul pe care îl pot suporta.
Acest principiu este folosit pentru a conecta celule de același tip în paralel în baterii atunci când este necesar să creșteți curentul la sarcină.Dar pentru a încărca un astfel de design, va fi necesar să creșteți puterea sursei. Această metodă este rar folosită pentru structuri gata făcute, deoarece acum este mult mai ușor să achiziționați imediat bateria necesară. Dar producătorii de baterii cu acid îl folosesc, conectând diferite plăci în blocuri individuale.
Conexiune serială
În funcție de materialele folosite, între cele două plăci electrozi ale bateriilor obișnuite în viața de zi cu zi se poate genera o tensiune de 1,2 / 1,5 sau 2,0 volți. (De fapt, această gamă este mult mai largă.) Evident, nu este suficientă pentru multe dispozitive electrice. Prin urmare, bateriile de același tip sunt conectate în serie, iar acest lucru se face adesea într-un singur caz.
Un exemplu de astfel de proiectare este dezvoltarea auto pe scară largă bazată pe acid sulfuric și plăci cu electrozi de plumb.
De obicei, în rândul oamenilor, în special în rândul șoferilor de transport, se obișnuiește să se numească baterie oricărui dispozitiv, indiferent de numărul elementelor sale constitutive - cutii. Cu toate acestea, acest lucru nu este în întregime corect.Structura, asamblată din mai multe cutii conectate în serie, este deja o baterie, pentru care este aplicată denumirea prescurtată «АКБ»... Structura sa internă este prezentată în figură.
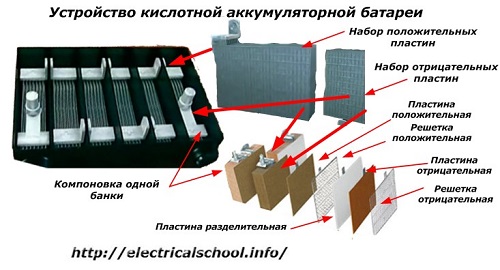
Fiecare dintre borcane este format din două blocuri cu un set de plăci pentru electrozii pozitivi și negativi. Blocurile se potrivesc între ele fără contact metalic, cu posibilitatea unei conexiuni galvanice fiabile prin electrolit.
În acest caz, plăcile de contact au o grilă suplimentară și sunt separate între ele printr-o placă separatoare.
Conectarea plăcilor în blocuri mărește suprafața lor de lucru, reduce rezistența totală a întregii structuri și vă permite să creșteți puterea sarcinii conectate.
Pe exteriorul cutiei, o astfel de baterie are elementele prezentate în figura de mai jos.
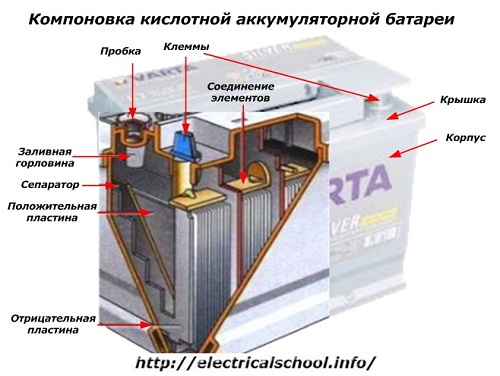
Acesta arată că carcasa robustă din plastic este etanșată cu un capac și echipată cu două terminale (de obicei în formă de con) deasupra pentru conectarea la circuitul electric al mașinii. Marcajele de polaritate sunt ștanțate pe terminalele lor: «+» și «-«. De obicei, terminalul pozitiv are un diametru puțin mai mare decât terminalul negativ pentru a bloca erorile de cablare.
Bateriile reparabile au un orificiu de umplere în partea de sus a fiecărui borcan pentru a controla nivelul electrolitului sau pentru a adăuga apă distilată în timpul funcționării. În el este înșurubat un dop, care protejează cavitățile interne ale carcasei de contaminare și, în același timp, împiedică vărsarea electrolitului atunci când bateria este înclinată.
Deoarece cu o încărcare puternică este posibilă gazarea din electrolit (și acest proces este posibil în timpul condusului intensiv), se fac găuri în dopuri pentru a preveni creșterea presiunii din interiorul cutiei.Prin ele ies oxigenul și hidrogenul, precum și vaporii de electroliți. Se recomandă evitarea unor astfel de situații care implică curenți de încărcare excesivi.
Aceeași figură arată legătura elementelor dintre bănci și dispunerea plăcilor cu electrozi.
Bateriile de pornire auto (acid cu plumb) funcționează pe principiul dublei sulfatări. În timpul descărcării/încărcării, asupra acestora are loc un proces electrochimic, însoțit de o modificare a compoziției chimice a masei active a electrozilor cu eliberarea/absorbția apei în electrolit (acid sulfuric).
Aceasta explică creșterea greutății specifice a electrolitului la încărcare și scăderea atunci când bateria este descărcată. Cu alte cuvinte, valoarea densității vă permite să evaluați starea electrică a bateriei. Pentru măsurarea acestuia se folosește un dispozitiv special - un hidrometru auto.
Apa distilată, care face parte din electrolitul bateriilor cu acid, se transformă într-o stare solidă - gheață la temperaturi negative.De aceea, pentru a preveni înghețarea bateriilor auto pe vreme rece, este necesar să se aplice măsuri speciale prevăzute de reguli. pentru exploatare.
Ce tipuri de baterii există?
Producția modernă pentru diverse scopuri produce mai mult de trei duzini de produse cu compoziții diferite de electrozi și electroliți. 12 modele cunoscute funcționează numai pe litiu.

Următoarele pot fi găsite ca electrod metalic:
-
conduce;
-
fier;
-
litiu;
-
titan;
-
cobalt;
-
cadmiu;
-
nichel;
-
zinc;
-
argint;
-
vanadiu;
-
aluminiu
-
alte elemente.
Acestea afectează caracteristicile de ieșire electrică și, prin urmare, aplicația.
Capacitatea de a rezista la sarcini mari pe termen scurt rezultate din rotirea arborilor cotiți ai motoarelor cu ardere internă de către motoarele electrice de pornire este caracteristică bateriilor cu plumb-acid. Sunt utilizate pe scară largă în transporturi, surse de alimentare neîntreruptibile și sisteme de alimentare de urgență.
Standard celule galvanice (baterii obișnuite) sunt de obicei înlocuite cu baterii nichel-cadmiu, nichel-zinc și nichel-hidrură metalică.
Dar modelele cu litiu-ion sau litiu-polimer funcționează în mod fiabil în dispozitive mobile și de calcul, instrumente de construcție și chiar vehicule electrice.
În funcție de tipul de electrolit utilizat, bateriile sunt:
-
acru
-
alcalin.
Există o clasificare a bateriilor în funcție de scop. De exemplu, în condiții moderne, au apărut dispozitive care sunt folosite pentru transferul de energie - reîncărcarea altor surse. Așa-numita baterie externă îi ajută pe proprietarii multor dispozitive mobile în absența unei rețele electrice alternative. Este capabil să încarce în mod repetat o tabletă, un smartphone, un telefon mobil.
Toate aceste baterii au același principiu de funcționare și un dispozitiv similar. De exemplu, modelul degetului cu litiu-ion prezentat în figura de mai jos repetă în multe feluri designul bateriilor cu acid discutat mai devreme.
Aici vedem aceiași electrozi de contact, plăci, separator și carcasă. Doar ele se fac tinand cont de alte conditii de munca.
Caracteristicile electrice de bază ale unei baterii
Funcționarea dispozitivului este afectată de parametrii:
-
capacitate;
-
densitatea energiei;
-
autodescărcare;
-
regim de temperatură.
Capacitatea se numește încărcare maximă a bateriei, pe care o poate oferi în timpul descărcării la cea mai mică tensiune. Este exprimat în pandantive (sistem SI) și amperi-ore (unitate non-sistem).
Ca tip de capacitate există „capacitate energetică”, care determină energia eliberată în timpul descărcării la tensiunea minimă admisă. Se măsoară în jouli (SI) și wați-oră (unități non-SI).
Densitatea de energie exprimată ca raport dintre cantitatea de energie și greutatea sau volumul bateriei.
Autodescărcare ia în considerare pierderea capacității după încărcare în absența unei sarcini pe terminale. Acest lucru depinde de proiectare și este agravat de defecțiunile izolației dintre electrozi din mai multe motive.
Temperatura de funcționare afectează proprietățile electrice și în cazul unor abateri grave de la norma specificată de producător, poate deteriora bateria. Căldura și frigul sunt inacceptabile, afectează cursul reacțiilor chimice și presiunea mediului din interiorul cutiei.
