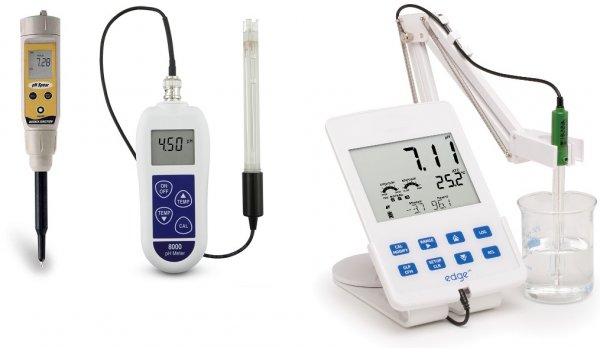
Principiul măsurării pH-ului, dispozitivul și tipurile de pH-metre
Pentru a determina rapid nivelul pH-ului (cu alte cuvinte, nivelul de aciditate) al diferitelor medii, se folosesc pH-metre. Apă industrială sau potabilă, soluție acidă, sare sau alcalină, sânge, urină și alte fluide corporale, fructe, legume și alte produse alimentare, medicamente medicale etc. — în principiu, totul poate deveni obiectul cercetării operaționale valoarea pH-ului.
Măsurarea pH-ului este în esență o măsurare a activității ionilor de hidrogen într-un mediu. Și chiar și denumirea pH în sine este tradus literal din latinescul „pondus Hydrogenii” ca „greutatea hidrogenului”.
Astăzi, pH-metrele sunt utilizate pe scară largă în microbiologie și medicină, în tratarea apei și agrochimie, în știința solului, în hidroponie, în cercetările de laborator și pe teren, în industria chimică și alimentară, în acvaristică și în multe alte locuri.
pH-metrul modern vă permite să determinați cu precizie și rapid valoarea pH-ului.Dacă pH-ul este 7, mediul este neutru, cum ar fi apa distilată, în care ionii pozitivi de hidrogen H + și ionii negativi de hidroxid OH- sunt împărțiți în mod egal. Dacă aciditatea este mai mare de 7, atunci mediul este alcalin. Dacă pH-ul este mai mic de 7, mediul este acid.
Și, deși chimiștii au reușit întotdeauna să determine aciditatea mediului prin metoda clasică, folosind indicatori, de exemplu, fenolftaleina, cu toate acestea, în unele procese este pur și simplu necesar să se cuantifice cu acuratețe acest indicator și, uneori, este necesar să se monitorizeze constant. aceasta, pentru a aranja să o corecteze. Pentru asta au fost inventate pH-urile.
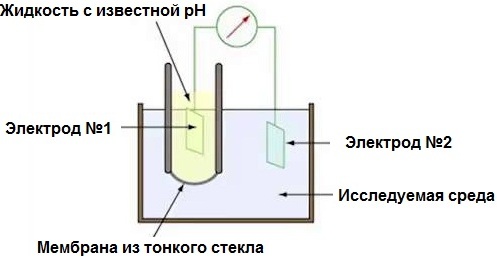
pH-metrul este de fapt un milivoltmetru electronic, deoarece măsoară diferența de potențial între sistemul electrochimic al unei perechi de electrozi și mediul de testare în care sunt plasați. Este adevărat că scara dispozitivului este gradată aici nu în milivolți, ci în pH, deoarece EMF măsurat se dovedește a fi proporțional cu pH-ul.
Doi electrozi: un indicator de sticlă (oxidanții nu se tem de sticla borosilicată) și clorură de argint - un electrod de referință suplimentar. Electrodul de sticlă are o rezistență foarte mare de zeci de megaohmi și aceasta este doar cerința de bază - rezistența sondei nu trebuie să fie mai mică de 0,1 GΩ. pH-metrul este calibrat folosind soluții tampon cu pH cunoscut.
Datorită faptului că valoarea EMF este afectată de temperatură, fiecare astfel de dispozitiv de măsurare are o compensare a temperaturii pentru măsurători la alte temperaturi decât + 25 ° C.Dar pentru a obține o precizie foarte mare, este necesar să se măsoare cu precizie la o temperatură de + 25 ° C, motiv pentru care multe pH-metre sunt echipate cu un termometru încorporat, astfel încât să puteți urmări imediat temperatura mediului în procesul de cercetare.
Electrodul din sticlă indicator sub formă de tub cu o bilă cu pereți subțiri la capăt, realizat dintr-o sticlă borosilicată specială conductoare de electricitate, este conectat în esență la un circuit electric. Mișcarea ionilor pozitivi H + în interiorul unui astfel de pahar face posibilă utilizarea acestuia (cationii din interiorul sticlei se mișcă în raport cu polianionul acidului silicic). În eprubetă se toarnă o suspensie de clorură de argint într-o soluție de acid clorhidric, după care se scufundă în ea un fir de argint - așa se obține un electrod de clorură de argint.
Electrodul de sticlă este coborât în mediul de testare, circuitul electric este închis prin introducerea unui electrod de referință suplimentar (pastă de mercur-calomel în soluție de clorură de potasiu) în el (prin intermediul unui comutator electrolitic sau direct). Clorura de potasiu creează contact între porțiunea de mercur-calomel a celulei și mediul de testare. Acest electrod suplimentar este de obicei plasat într-o carcasă de sticlă care este impermeabilă la ionii H +.
Contactul conductiv al soluției de clorură de potasiu din electrodul de referință cu soluția de testat se formează datorită unui fir subțire sau capilar într-o carcasă de sticlă.În acest fel, se obține o celulă galvanică dintr-un electrod de referință și un electrod de clorură de argint și partea electrolit a celulei include o peliculă de sticlă conductivă și un mediu de testare.
EMF-ul sistemului de electrozi este măsurat cu un milivoltmetru, scara sa este gradată în pH.Electronii de la electrodul de clorură de argint sunt transferați la electrodul de referință sub acțiunea EMF măsurată, care este întotdeauna însoțită de transferul unui număr egal de protoni din interiorul electrodului de sticlă către mediu.
Dacă în acest caz luăm concentrația ionilor pozitivi de hidrogen H + în constanta electrodului de sticlă, atunci EMF va fi o funcție de activitatea lui H +, adică o funcție de pH-ul mediului studiat.
Modelele moderne de pH-metre funcționează datorită microprocesoarelor care efectuează compensarea temperaturii și rezolvă multe sarcini conexe. Cu cât dispozitivul este mai complex, cu atât poate rezolva mai multe sarcini. Clasa de precizie a instrumentelor variază în funcție de model și poate fi selectat un pH-metru potrivit pentru diferite aplicații.
Există pH-metre de buzunar de uz casnic, sunt de laborator profesionale, portabile și staționare industriale. Unele pH-metre măsoară concentrația de ioni în mediu, conținutul de nitrați etc., au o memorie încorporată pentru stocarea rezultatelor, capacitatea de a comunica cu un computer și funcția de ajustare a parametrilor printr-o buclă de feedback.